MI PRIMER LABORATORIO DE CIENCIAS EN CASA
La temporada de cuarentena en medio de la pandemia por coronavirus nos desafía a planear nuevas actividades con los chicos, poco acostumbrados a tantos días de encierro. Los juegos de mesa se agotan, las pantallas tienen un limitado tiempo de uso recomendable y no siempre hay espacio para movimientos más deportivos. La ciencia puede ser otra gran opción: con experimentos sencillos, los niños tienen la posibilidad de convertirse en científicos, al menos por un rato.
Para nuestro primer laboratorio vamos a necesitar:
Una mesa para poner todos los materiales que vamos a utilizar.
Una bata de laboratorio, es opcional (ropa de estar en casa)
Arena
Limaduras de hierro y pedazos de hierro (por lo general lo regalan en los talleres)
Harina
Hielo
Olla (pequeña)
Vasos de cristal o desechables transparentes
Cernidor pequeño
Guantes quirúrgicos (en la tienda se consiguen)
Filtro de papel desechables (se usan en cafeteras cafetera)
Toallita o un paño que no uses, (para limpiar y secar tus manos)
Agua
Aceite
Imán (es opcional)
Cafe (un sobresito instantaneo)
Limón
Tres o dos frutas picadas
Sal
Azúcar
Colorante (opcional)
Un globo (una bomba R12)
Dos cucharas desechables
Una paleta para revolver ( de esas de paleta, es opcional)
Vinagre
Bicarbonato
Una hoja de repollo morado
¿Qué es una mezcla?
En química, una mezcla es un material compuesto por dos o más componentes unidos físicamente, pero no químicamente. Esto último significa que no se produce entre ellos ninguna reacción química. Por eso, que cada componente mantiene su identidad y sus propiedades químicas, incluso en el caso en que no podamos distinguir un componente del otro.
Los componentes o fases de una mezcla se hallan unidos mecánica o físicamente. Por eso, a menudo se ven alteradas sus propiedades físicas, como el punto de ebullición.
Sin embargo, al no producirse cambios químicos permanentes, es posible emplear mecanismos físicos de separación para extraer cada uno de los componentes de una mezcla. Dichos mecanismos físicos suelen ser térmicos (cuando involucran calor) o mecánicos (cuando involucran el desplazamiento o el movimiento).
Las mezclas son formas mixtas de la materia sumamente frecuentes en la vida cotidiana, y muchos de los materiales que usamos son fruto de un procedimiento de mezclado o mixtura. Los componentes de una mezcla pueden hallarse en distinto estado de agregación, ya sean sólidos, líquidos, gaseosos o plasmas, así como combinaciones entre ellos.
Ensalada de frutas
¿Qué son los métodos de separación de mezclas?
 Los métodos de separación de mezclas o métodos de separación de fases son los distintos procedimientos físicos que permiten separar dos o más ingredientes de una mezcla, valiéndose de las diferentes propiedades químicas de cada uno de ellos.
Los métodos de separación de mezclas o métodos de separación de fases son los distintos procedimientos físicos que permiten separar dos o más ingredientes de una mezcla, valiéndose de las diferentes propiedades químicas de cada uno de ellos.
Nótese entonces que, para que estos mecanismos funcionen, debe tratarse de mezclas en que los ingredientes conserven su identidad, y no haya habido reacciones químicas que alteren sus propiedades permanentemente o den origen a nuevas sustancias. Rasgos como el punto de ebullición, la densidad o el tamaño deben conservarse en los ingredientes para que puedan aplicarse los métodos de separación de mezclas.
En cambio, estos métodos funcionan sin distingo en mezclas homogéneas
y heterogéneas, ya que no suponen tampoco ningún cambio en la identidad de los ingredientes (elementos que conforman la mezcla), que pueden así recuperarse más o menos como estaban antes de realizar la mezcla. Dependiendo del método aplicado, se lograrán ingredientes originales con más o menos pureza.
¿Qué es una mezcla homogénea?
Una mezcla homogénea es una unión de dos o más sustancias que forman un material conjunto, en el cual son indiferenciables los dos elementos originales, aun cuando no se hallan químicamente unidos. Dicho más fácilmente: los elementos que componen la mezcla homogénea no pueden diferenciarse a simple vista, pero son separables físicamente, pues entre ellos no tiene lugar una reacción química.
Las mezclas son materiales de uso muy común en la rutina de la humanidad, en aspectos tan diversos como la cocina, la construcción y un gigantesco etcétera.
Para lograr una, basta con unir mecánicamente dos o más sustancias distintas, hasta que formen una materia conjunta: los ingredientes se juntan pero conservan sus propiedades químicas y, generalmente, pueden ser separados de nuevo, a través de procedimientos como el tamizado, la filtración, la separación magnética, la decantación o la centrifugación, entre otros.
Una mezcla puede consistir en elementos tanto en estado líquido, sólido o gaseoso, y por lo general forman aleaciones (cuando se involucra metales), soluciones (cuando el ingrediente predominante es líquido), suspensiones (cuando se encuentra un sólido mezclado en un líquido o gas) o coloides (sólidos muy finos en una fase líquida).
Debido a las razones arriba explicadas, las mezclas no forman nuevos compuestos, sino que constituyen una juntura de sus ingredientes.
¿Qué es una mezcla heterogénea?
Una mezcla heterogénea es un material compuesto por la unión de dos o más sustancias no vinculadas químicamente. No es fruto de ningún tipo de reacción química, aunque la mezcla en sí misma puede dar lugar a algún tipo de reacciones posteriormente. Su característica fundamental es que sus componentes suelen distinguirse fácilmente entre sí.
Una mezcla heterogénea puede estar compuesta por sólidos, líquidos o gases, o combinaciones entre ellos. Generalmente se produce mediante procedimientos mecánicos de mezclado, durante los cuales no se producen cambios significativos en las sustancias integrantes de la mezcla.
Sin embargo, aunque las sustancias retienen sus identidades, la mezcla puede dar pie a suspensiones, coloides, aleaciones y otras formas en las que no resulte tan sencillo separarlas.
Para ello, justamente, existen los mecanismos de separación de mezclas, que son usualmente procedimientos físicos a través de los cuales pueden separarse estos componentes, como son:
Filtración
Útil para separar sólidos no solubles de líquidos, consiste en la utilización de un filtro (papel filtrador, piedras filtrantes, etc.) que permite el paso del líquido por porosidad pero retiene los elementos sólidos. Así operan los filtros de agua de nuestras casas, o el papel filtro donde vertemos el café sólido antes de verterle encima el agua caliente: el agua surge del papel mezclada con lo más fino del café, y las partes gruesas se desechan junto con el filtro.
EBULLICIÓN Y EVAPORACIÓN
La realidad dicta que los procesos que pueden llevar un líquido a estado gaseoso son dos: ebullición y evaporación. En este caso, la evaporación es el proceso de transición en el que un líquido pasa a estado gaseoso. La evaporación se refiere al proceso que ocurre justo sobre la superficie entre el líquido y el gas.
Para no confundirla con la ebullición, hay que tener en cuenta el proceso. En la evaporación, se da solo en la superficie del líquido. Mientras, la ebullición se da en la totalidad del líquido. Es un proceso endotérmico, pues necesita de calor para transicionar a gaseoso.
Cristalización
Ideal para separar sólidos disueltos en líquidos (sal en agua, azúcar en agua, etc.), consiste en evaporar el líquido hasta obtener en el fondo del recipiente los cristales del sólido disuelto. Es así como se obtiene la sal marina, por ejemplo. Dependiendo de la velocidad de la evaporación, los cristales serán más grandes o más chicos.
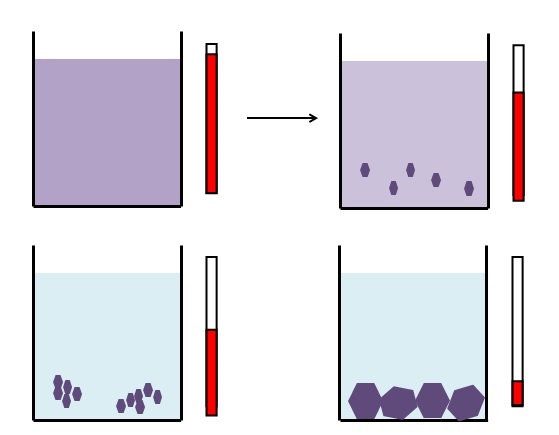
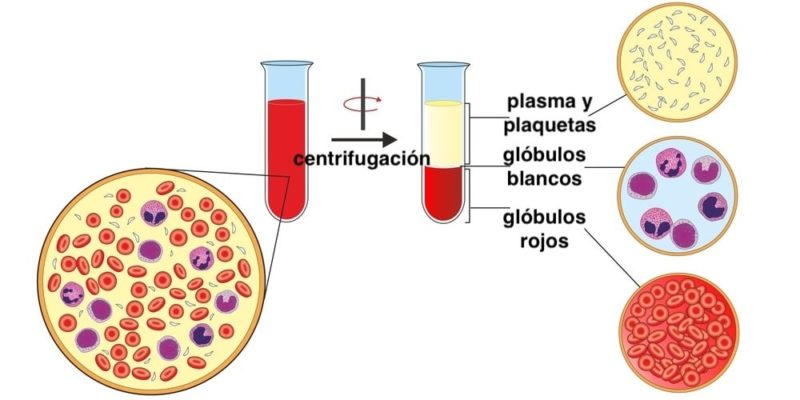
¿Qué es la centrifugación?
La centrifugación es un mecanismo de separación de mezclas(en particular, las compuestas por sólidos y líquidos de distinta densidad) a través de su exposición a una fuerza giratoria de determinada intensidad.
Esta fuerza, conocida como fuerza centrífuga en la mecánica newtoniana, es una fuerza ficticia que aparece cuando un cuerpo describe un movimiento de rotación. Su nombre quiere decir “que huye del centro”, pues se aleja del eje de rotación de la trayectoria del cuerpo.
La fuerza centrífuga hace que los objetos se alejen del centro al girar. Por ejemplo: cuando un pescador hace girar el anzuelo antes de arrojarlo al mar, o la fuerza que nos empuja contra el asiento en las atracciones giratorias de los parques de diversiones. Es la misma que emplea una centrifugadora, o aparato capaz de generar fuerza centrífuga, para separar mezclas en un laboratorio.
La centrifugación opera empujando los componentes más densos de la mezcla hacia el punto más alejado del eje de rotación y dejando los menos densos en el punto más cercano. Esta técnica es de uso cotidiano por químicos, biólogos y otros científicos.
¿Qué es la destilación?
Se denomina destilación a un método de separación de fases, también llamados métodos de separación de mezclas, que consiste en el uso consecutivo y controlado de otros dos procesos físicos: la vaporización (o evaporación) y la condensación, usándolas de manera selectiva para separar los ingredientes de una mezcla por lo general de tipo homogéneo, es decir, en la que no pueden distinguirse a simple vista sus elementos.
Las mezclas susceptibles a destilación pueden contener dos líquidos, un sólido en un líquido o incluso gases licuados, puesto que este método aprovecha el punto de ebullición de las sustancias, una de las características inherentes a la materia.
El punto de ebullición es, entonces, la temperatura precisa a la cual un líquido pasa a convertirse en gas (es decir, se evapora).
De este modo, para que la destilación se lleve a cabo correctamente, deberemos hervir la mezcla hasta alcanzar el punto de ebullición de una de las sustancias integrantes, que entonces pasará a ser vapor y podrá ser conducido hasta un recipiente enfriado, en el cual condensarse y recuperar su liquidez.
La otra sustancia integrante, en cambio, permanecerá en el recipiente sin alteraciones; pero en ambos casos tendremos sustancias puras, libres de la mezcla inicial.
La combustión es una reacción química que libera energía lumínica y calorífica.
¿Qué es la destilación?
Se denomina destilación a un método de separación de fases, también llamados métodos de separación de mezclas, que consiste en el uso consecutivo y controlado de otros dos procesos físicos: la vaporización (o evaporación) y la condensación, usándolas de manera selectiva para separar los ingredientes de una mezcla por lo general de tipo homogéneo, es decir, en la que no pueden distinguirse a simple vista sus elementos.
Las mezclas susceptibles a destilación pueden contener dos líquidos, un sólido en un líquido o incluso gases licuados, puesto que este método aprovecha el punto de ebullición de las sustancias, una de las características inherentes a la materia.
El punto de ebullición es, entonces, la temperatura precisa a la cual un líquido pasa a convertirse en gas (es decir, se evapora).
De este modo, para que la destilación se lleve a cabo correctamente, deberemos hervir la mezcla hasta alcanzar el punto de ebullición de una de las sustancias integrantes, que entonces pasará a ser vapor y podrá ser conducido hasta un recipiente enfriado, en el cual condensarse y recuperar su liquidez.
La otra sustancia integrante, en cambio, permanecerá en el recipiente sin alteraciones; pero en ambos casos tendremos sustancias puras, libres de la mezcla inicial.
El carbón utiliza la destilación en seco para obtener combustibles orgánicos líquidos.
¿Qué es la decantación?
Se conoce como decantación a un procedimiento físico que sirve para separar una mezcla compuesta por un sólido o un líquido de mayor densidad, y un líquido de menor densidad.
La separación ocurre inicialmente por acción de la gravedad terrestre, que atrae con mayor fuerza a la sustancia densa y la lleva hacia el fondo de un envase, permitiendo al líquido menos denso ocupar la porción superior del mismo. Entonces se procede a derramar o extraer del envase el elemento inferior.
Este proceso es ampliamente utilizado en laboratorios y procesos industriales, sobre todo mediante embudos de decantación o herramientas similares. No se lo debe confundir con la sedimentación o separación gravítica, que consiste en la separación de residuos sólidos suspendidos en un líquido (como agua y arena) por el mero efecto de la gravedad.
Existen dos formas en que puede llevarse a cabo la decantación, atendiendo al estado de las sustancias que integran la mezcla:
- Decantación sólido-líquido. Cuando se encuentran elementos sólidos depositados en un medio líquido.
- Decantación líquido-líquido. Cuando la mezcla se forma por dos líquidos de densidades diferentes y que no pueden disolverse el uno en el otro (mezcla heterogénea).
En la decantación del vino se extraen los sedimentos y se oxigena el vino.
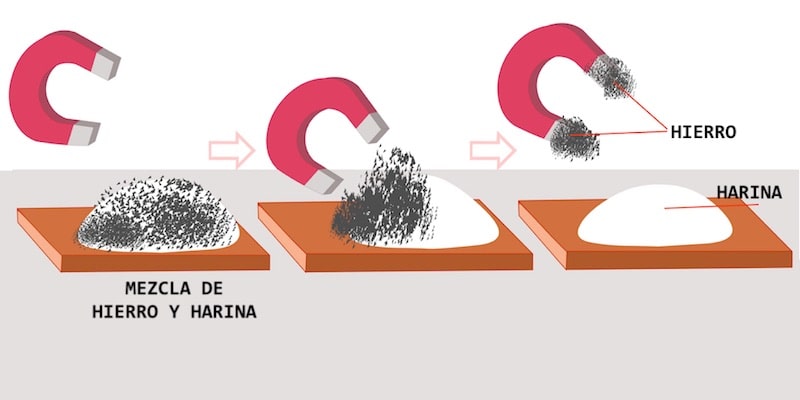
Separación magnética
Consiste en la separación de fases de acuerdo a su potencial magnético. Algunas sustancias responden a los campos magnéticos y otras no, y de acuerdo a dicha diferencia se aplica un imán o electroimán a la mezcla, permitiéndole atraer un ingrediente y dejar el otro intacto (fragmentos de hierro en tierra, mercurio en agua, trozos de metal en agua, etc.).
Cromatografía
Útil para separar mezclas complejas que no responden a ningún otro método, empleando la capilaridad como principio: aquél que permite el avance de una sustancia a través de un medio específico. Se identifica así a las dos fases de la mezcla como fase móvil (la que avanza sobre la otra) y fase estacionaria (sobre la que se avanza). Por ejemplo, al derramar café sobre una tela, el primero tiende a avanzar ocupando la superficie toda de la segunda.
Para que ello ocurra debe haber cierta atracción entre ambas fases, y de acuerdo a ella, el movimiento se dará más rápido o más lento. A través de un cromatógrafo (en papel o en máquina), puede medirse la cantidad de móvil sobre la estacionaria, estudiando el color que adquiere la mezcla.
Tinta de repollo
Este experimento tiene que ver con los indicadores ácido base.
Se necesitan hojas de repollo colorado, un poco de vinagre o jugo de limón, bicarbonato de sodio, agua, cucharitas y vasos.
Hay que romper las hojas de repollo colorado (puede ser con la mano) y ponerlas en un recipiente. Una persona adulta vuelca agua bien caliente en ese recipiente. Lo que va a pasar es que el agua se va a empezar a teñir de violeta. Ahí lo que estamos haciendo es extraer los pigmentos, que son las sustancias que le dan color a la hoja de repollo. Esos pigmentos se llaman antocianinas y tienen una particularidad: cambian de color dependiendo de la acidez del medio. Entonces, si están en un medio ácido, se ponen de color fucsia brillante; y si están en un medio básico, se ponen de color verde o azul. Por eso los llamamos indicadores ácido base, porque nos sirven para saber si estamos en un medio ácido o básico.
Inflar globos sin soplar
Otro posible experimento es el de inflar globos sin soplar. Lo que hay que hacer es poner en la botella un fondito de vinagre. Dentro del globo, unas cucharaditas de bicarbonato de sodio. Lo que hay que hacer es colocar la boca del globo en la boca de la botella, volcar el bicarbonato dentro del vinagre y sostener. Lo que va a pasar es que el vinagre tiene ácido acético y el bicarbonato es una base. Cuando reaccionan, se libera un gas. Ese gas inflará el globo.
Una vez que esté inflado, lo pueden atar y ese globo se porta diferente. Como no está lleno de aire, sino de dióxido de carbono, que es más denso, cae más rápido. ¡A jugar con la ciencia!














Comentarios
Publicar un comentario